- HOME>
- ネオアンチゲンを使った樹状細胞治療
遺伝子解析による免疫細胞治療/個別化医療
〜遺伝子解析による個別化がん免疫細胞治療法〜
がんは遺伝子(DNA)の異常によって起こる病気です。
遺伝子異常からできるタンパク質は“ネオアンチゲン”といわれ、がん細胞にしか発現していないため、免疫細胞治療の強い攻撃目標となります。
遺伝子解析後、遺伝子異常を持つネオアンチゲンを合成し、患者さんの樹状細胞と反応させ、反応後患者さんに注射します。患者さん固有の遺伝子異常を持つネオアンチゲン(がん抗原)を合成するため、個別化医療、オーダーメイド医療を実現できます。
ネオアンチゲン樹状細胞治療の流れ
①Aさんのがん細胞の遺伝子(DNA,RNA)を調べる!(約1ヶ月)

※左右にスクロールして確認することができます。
②異常遺伝子の情報からネオアンチゲン(がんの目印)を合成する。(約3週間)
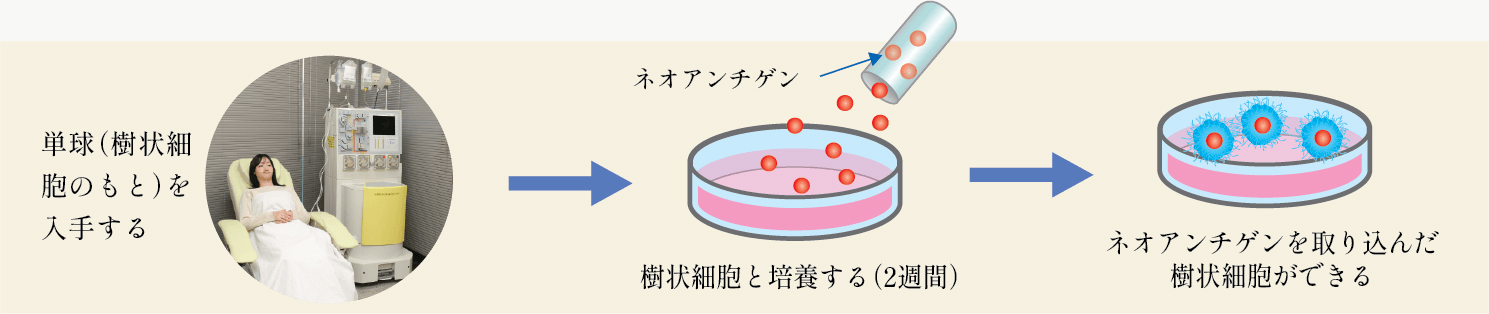
③成分採血
※左右にスクロールして確認することができます。
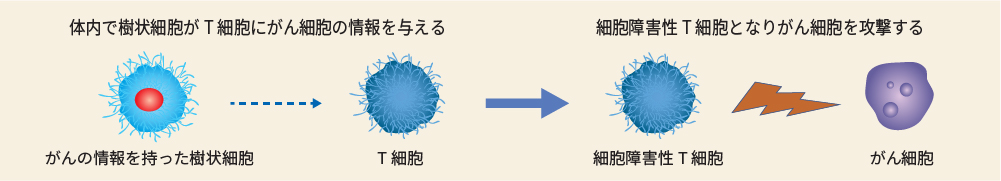
④Aさんだけのオリジナル樹状細胞ワクチンができる。

⑤皮下注射する。(2週間に1回×6回)
※左右にスクロールして確認することができます。
成分採血
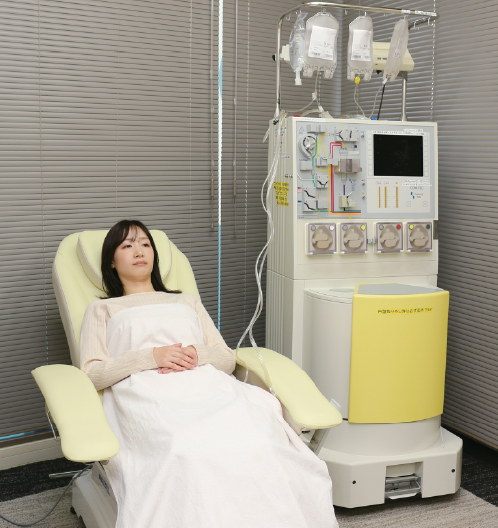
体外で血液を循環させながら
樹状細胞やNK細胞の元となる単球を含む
必要な成分だけを採る
アフェレーシス(成分採血)という方法です。
体外で免疫細胞に育てる
採取した血液から単球を取り出し、
培養して樹状細胞やNK細胞を育てます。
成分採血の長所
(メリット)
一度に多量の免疫細胞の元となる
単球を採取できます。
